再生医療用材料の設計
細胞親和性インジェクタブルゲル (Injectable Hydrogels)
再生医療の大きなテーマのひとつは、「損傷した組織の中で細胞がしっかり生きられる環境をいかに作るか」です。細胞はただ培養皿に置くだけでは組織を形成することができず、周囲に適切な足場や水分環境が整って初めて機能の再生が可能となります。そのため、損傷組織に直接 “細胞の足場” を注入できる材料として、インジェクタブルゲル(注射可能なゲル) が注目されています。
インジェクタブルゲルは、注射器で注入できるほど柔らかい状態で体内に導入し、体温や生体環境、化学反応をきっかけにゲル化して固まり、細胞を包み込むようにして留まります。この仕組みにより、手術を伴わない低侵襲な治療を実現しつつ、細胞を目的部位にしっかり固定することができます。
松村研究室では、独自の高分子技術を用いて 「細胞に優しく、必要なときにだけゲル化する」 材料を開発しています。特に強みとなっているのが、反応性多糖類です。多糖にアルデヒドやメタクリル基などの反応性部位を導入し、ポリリジンやゼラチンなどと反応させてゲル化します (図8)。
これらのインジェクタブルゲルは、分子設計によってゲル化のタイミングや力学特性を制御できる点も大きな特徴です。注入時は低粘度であるため操作性が高く、体内に入ると適切な強度を持つゲルとなって細胞を保持します。論文では、ゲル内部の微細構造を調整することで、細胞の浸潤速度や増殖挙動をコントロールできることが示されています (Jain M., et al., Mater. Sci. Eng. C, 2016)。
また、反応性のゲルは生体接着剤としての応用も期待されます。手術後の止血や縫合の補助などに利用することができます (Matsumura K. et al., Carbohydr. Polym. 2014, Hyon W., et al., Carbohydr. Polym., 2022)。
インジェクタブルゲル研究は、化学・物性・細胞生物学が交差する総合領域であり、高分子材料の合成から、ゲル物性解析、細胞評価まで一貫して体験できます。将来的には、軟骨再生、筋再生、皮膚治療、薬剤放出システムなど、多様な医療応用が期待される分野です。新しい医療材料を“自分で作れる”やりがいのある研究テーマです。
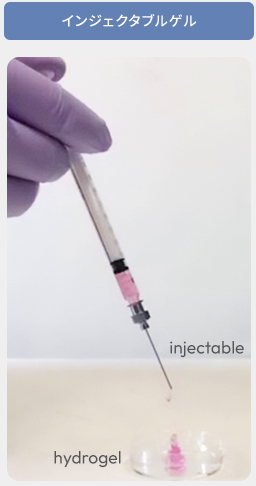
注射針を通るときは溶液で、その後ゲル化する。
分解性多糖による足場材料 (Biodegradable Polysaccharide Scaffolds)
再生医療では、細胞を体内で増やし、最終的に組織として再生させるための「足場(スキャフォールド)」が不可欠です。
足場は細胞が付着・増殖・移動できる“家”の役割を果たしつつ、体内に長く残りすぎず、適切なタイミングで分解されて消えていく必要があります。
しかし、多くの合成高分子は分解されませんし、生体に安全なタンパク質や多糖類などは分解の制御が困難という課題があります。
松村研究室では、この課題を解決するために、化学的に分解性を付与した新しい多糖スキャフォールドを開発しています。その核となるのが、Malaprade酸化を 利用した分子改質です。この反応では、多糖のグルコース単位に存在する1,2-ジオールが選択的に酸化され、アルデヒド基を導入することができます。
このアルデヒド基は、生体内に存在するアミノ基(タンパク質・ペプチド・細胞外マトリックスなど)と反応してシッフ塩基結合を形成します。この反応自体は
可逆的で、環境によって結合と解離が繰り返されますが、このプロセスの中で主鎖が切断され、徐々に分解が進むことが松村研の研究によって明らかになりました。
つまり、「アルデヒド導入量=分解速度の制御スイッチ」になるという革新的なコンセプトです
(図9,Chimpibul W. et al., J. Polym. Sci. A. 2016, Nonsuwan, P et al., Carbohydr. Polym. 2019)。

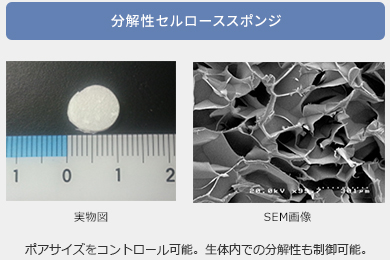
実際に論文では、酸化度を変化させたセルローススキャフォールドの分解挙動、細胞適合性、タンパク質吸着性、炎症反応について詳細な検討が行われています (図10, Chimpibul W. et al., J. Mater. Chem. B, 2020)。酸化度が高すぎると過剰なタンパク質反応性により炎症が起こりやすくなり、逆に低すぎると分解が遅くなります。最適な酸化度を選ぶことで、生体内で穏やかに吸収され、同時に細胞増殖を促す理想的な足場材料を作ることができることが示されました。
また、松村研では多糖スキャフォールドの多孔構造の制御にも取り組んでいます。 塩析法によって得られた多孔性セルロースの三次元構造は、細胞が浸潤するうえで重要な「高い空隙率」と「連続した孔」を持ち、組織再生のための栄養拡散や細胞移動をサポートします。学生は、材料の化学修飾、構造解析(SEM、NMR)、細胞実験、さらには in vivo 評価まで、多面的な研究を経験できます。
多糖由来スキャフォールドは、安全性・分解性・細胞適合性のバランスを自在に調整できる点が大きな魅力で、医療材料として非常に将来性の高い分野です。創傷治癒、軟部組織再生、ドラッグデリバリー、止血材など、多彩な応用が広がっています。