常識にとらわれない新しい発想で医療に貢献する
バイオマテリアルが対象とする研究範囲は大変広く、多分に学際的といえます。
マテリアルですから材料工学、化学、物理がベースと成っていることは言うまでもないでしょう。応用対象が生体であるため、生物学や医学の知識も必要です。生体計測やイメージング、シミュレーションなどの医工学分野では情報学やコンピュータの助けも必要かもしれません。そのような幅広い研究対象の中で、私の研究室で興味を持って取り組んでいるいくつかのテーマについて紹介します。
本研究室では高分子化学に立脚し、一般的な常識にとらわれない新しい発想で医療に貢献するような材料開発に関わる研究を順次拡大していく予定です。
両性電解質高分子化合物を利用したバイオマテリアル
生体の60%は水と言われています。生体内の反応場は主に水溶液です。タンパク質など生体高分子は水溶液中で非常に多様で重要な振る舞いをします。近年、タンパク質のモデル化合物として正、負の両方の電荷を持った高分子 ( 両性電解質高分子 ) の研究が注目されつつあります。私の研究室では両性電解質高分子の特異的性質を調べ、その材料応用を目指しています。
1. 細胞凍結保護効果
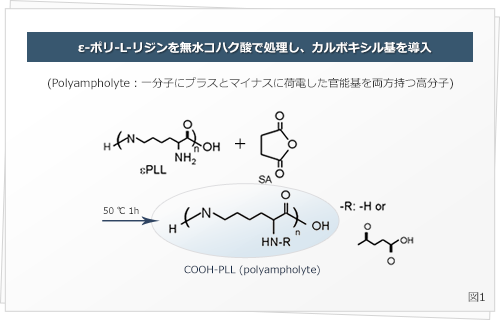
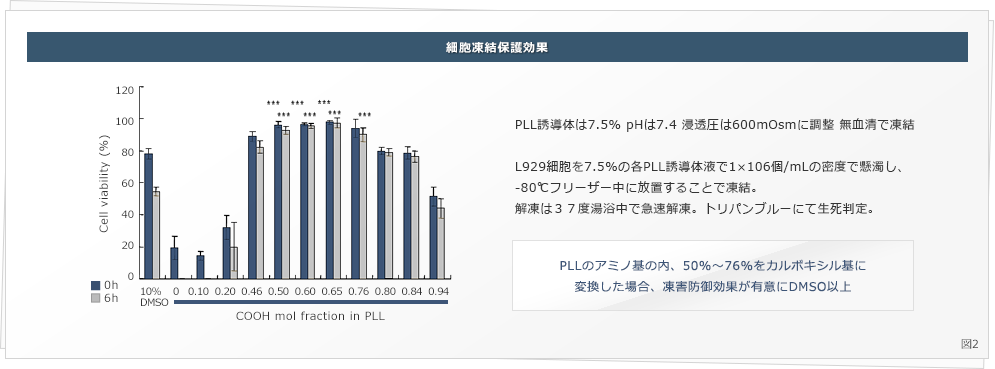
ポリリジンのアミノ基を一部カルボキシル基に変換した、両性電解質高分子 (図1) の水溶液中に細胞を懸濁して凍結することで、細胞の生存率を高く保ったまま凍結保存できることを明らかにしました。
( (図2) Matsumura K. et al., Biomaterials 2009 )
この機能は種々の細胞の凍結保護に有効で、幹細胞やヒトiPS細胞の凍結保存にも有用であることを示しました。
( Matsumura K. et al., Cell Transplantation 2010, Matsumura K. et al., Cryobiology 2011 )
凍結保護の機序解明
このように、それのみで細胞を高効率に凍結保存できるような高分子化合物はこれまでに報告されておらず、その機序の解明に興味が持たれます。
我々はその機序の解明のため、いくつかの研究を行っています。
低温における高分子溶液の挙動解析
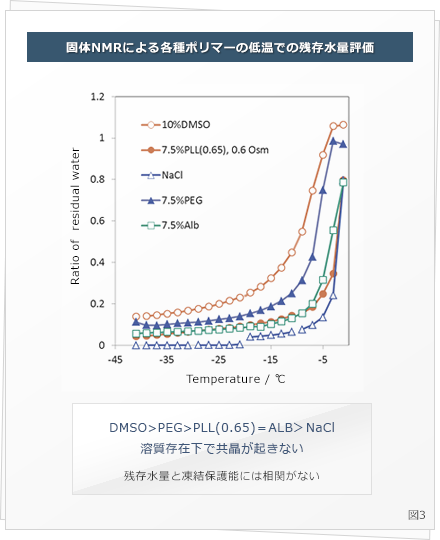
凍結状態での高分子間、高分子-水間、高分子-塩間の相互作用を固体NMRを用いて調べています。この手法により、凍結時の細胞外環境の変化に対する両性高分子電解質の影響から機序の解明を目指しています。
図3では、種々の高分子水溶液を凍結した時の氷中の残存水の割合を示しています。この結果よりカルボキシル化ポリリジンは必ずしも残存水を多く保持しているわけでは無いことがわかり、残存水 (高分子による束縛水) の効果だけでは凍結保護作用が説明できないことがわかります。
そこで、23Na-NMRを用いて塩 ( Naイオン ) と高分子との低温での相互作用を調べると、低温でNaのシグナルが小さくなることがわかりました。
このことから、Naイオンの運動性が低下し、固体状態に近い状態を取っていることが示唆されます。すなわち、両性電解質高分子の側鎖の電荷にNaイオンがトラップされることにより凍結による急激な浸透圧の上昇を防いでいる効果がある可能性があります。このようにこれまで知られていなかった凍結保護作用に関して材料学的見地から新たな知見を見いだす研究を行っています。
合成凍結保護高分子の設計
カルボキシル化ポリリジンだけでなく、プラスのモノマーとマイナスのモノマーを共重合させた、完全合成の両性電解質高分子にも凍結保護効果があることを報告しました ( Rajan R., et al., J. Biomater. Sci. Polym. Ed., 2013 ) 。
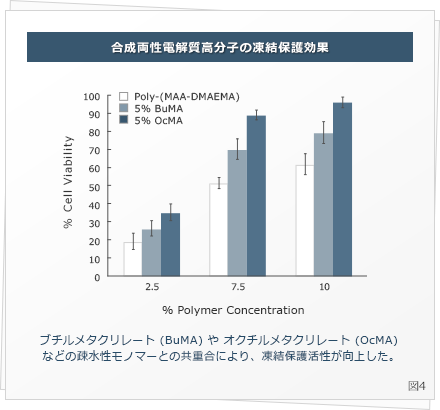
たとえば、第3級アミノ基をもつモノマーとカルボキシル基を持つモノマーを共重合させた両性電解質高分子は、高い細胞凍結保護活性を持ちましたが、一方で、側鎖に両方の電荷を持つ双性イオン高分子(zwitterionic ppolymer)は高い活性を持ちませんでした。
その機序として、各ポリマーが持つ細胞膜親和性や、氷晶成長抑制効果の違いが関与していることがわかりました ( Rajan R. et al., Biomacromolecules, 2016 ) また、ブチルメタクリレートなどの疎水性のモノマーを少量共重合することでさらに保護活性が向上することも報告しました (図4) 。
このように、分子設計により、新しい凍結保護物質の最適化も可能となってきています。将来的には、細胞ごとに最適なテイラーメイドの凍結保護剤の開発も可能になるかもしれません。
再生医療用細胞シートの凍結保存
再生医療の研究が広がるにつれ、細胞構造体の創出が容易になってきています。たとえば、細胞シートや再生皮膚、再生軟骨などの開発が盛んに行われ、すでに臨床応用も行われています。iPS細胞などの幹細胞から組織を作成することが可能となりつつありますが、まだまだ時間がかかります。そこで、できあがった組織をあらかじめ凍結してストックしておくという技術があると、必要な時に必要な組織をすぐに使用することができます。そのような技術があれば、再生医療の産業化が見えてきます。
しかし、細胞懸濁液と異なり、細胞のシートや構造体は、細胞ー細胞間の相互作用があり、また大きな構造体であることから、一般的な-80℃に放置するという緩慢凍結法では生存率を維持できないという問題があります。そこで、受精卵などの凍結保存に用いられているガラス化法 ( Vitrification ) という手法に着目しました。
ガラス化法は、超急速凍結を行うことで、凍結時に水の結晶化を防ぎ、アモルファスのまま固化させるという手法です。この手法によると、細胞内外の水の体積膨張や、結晶による物理的ダメージなどを防ぐことができます。ただし、水は非常に結晶化しやすいので、結晶化を防ぐために高濃度の溶質、非常に速い凍結速度が要求されてきました。
当研究室で開発した両性電解質高分子化合物に、氷晶の成長を抑制するという研究成果が報告されました ( Vorontsov D., et al., J. Phys. Chem. B., 2014 ) 。そこで、当研究室では、カルボキシル化ポリリジンの氷晶成長抑制効果を調べ、より効果的なガラス化保存液の開発を行っています。具体的には、低濃度の溶質でより簡便に誰でもできる手法を開発し、それを再生医療用の細胞構造体の凍結へ応用したいと考えています。
軟骨シートのガラス化 Maehara M., et al., BMC Biotechnol., 2013
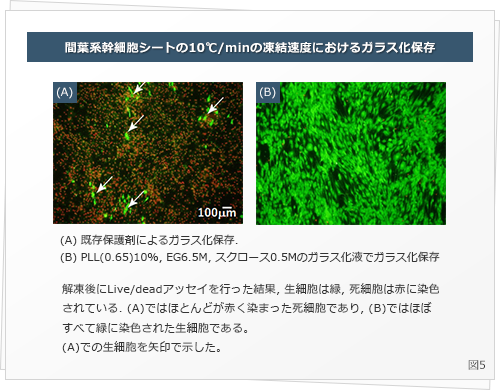
間葉系幹細胞シートのガラス化 Matsumura K., et al., ACS Biomater. Sci. Eng., 2016 (図5)
2. 足場材料への応用
バイオマテリアルが人工臓器から再生医療へとその応用領域を広げつつあります。
例えば三次元足場材料の上で幹細胞を培養したりすることで生体内環境を模倣し、移植後の生着率や組織再生能を向上したり、分化を制御したりするような研究が盛んになされています。
我々は例えば両性電解質高分子を架橋し、ゲル化させることにより細胞を凍結保存可能な足場材料を創出しました ( Jain M. et al., Biomater. Sci. 2014, Jain M. et al., J. Biomed. Mater. Res. A. 2016, Jain M. et al., Mater. Sci. Eng. C., 2016 ) 。また、両性電解質高分子表面はタンパク質や細胞の接着を抑制することが報告されており、その性質を用いて種々の有用なバイオマテリアル表面を設計することに興味を持っています。
3. タンパク質の凝集抑制作用
タンパク質は、生体を構成する主要な有機化合物であり、多種多様な機能を持っています。その機能はタンパク質自身の構造と大きな関係があります。つまり、構造が失われると機能も損なわれることが多いのです。たとえば、リゾチームは卵の白身の成分ですが、熱をかけると白く固まります。リゾチームは抗菌活性をもつタンパク質ですが、熱で凝集したリゾチームには活性がなくなります。そこで、凝集を抑え、活性を維持するとタンパク質凝集抑制剤の研究が盛んに研究されています。
当研究室では、双性イオン高分子であるポリスルホベタインに、高いタンパク質凝集抑制能があることを報告しました ( Rajan R, Matsumura K., J. Mater. Chem. B., 2015 ) 。図6にあるように、ポリスルホベタインを添加した場合、リゾチームを90℃で30分熱しても凝集塊ができずに、酵素活性を維持していることがわかりました。この作用は、ポリスルホベタインをナノゲルにしたり、疎水性基を導入することでさらに増強することもわかり ( Rajan R, Matsumura K., Sci. Rep., 2017 ) 、様々なタンパク質・酵素の凝集抑制作用について応用展開が考えられます。
最近ではインスリンの凝集抑制にも大きな効果を示すことを報告しました ( Rajan R. et al., Macromol. Biosci., 2018, Sharma N. et al., ACS Omega 2019 ) 。

4. 相分離構造の解明とその応用

カルボキシル化ポリリジン水溶液はそのカルボキシル基導入量により、液液相分離構造を有することがわかりました。また、相分離は溶液濃度と塩濃度に大きく左右され、温度応答性もあることがわかっています。濃厚水溶液の状態では1相で安定なのですが、水で薄めるとある濃度以下では液液相分離します。
この相分離は塩を加えると解消されることから、両性電解質高分子の側 鎖の電荷によるポリイオンコンプレックスの形成によるものと考えられます。つまり濃縮相は、水溶液で有りながらこれ以上薄められないという一見不思議な性質を持っているのです。この性質の詳細を解明するとともに、表面修飾やゲル、粒子などのバイオマテリアルへの応用を検討しています (図7) 。
カルボキシル化の際に使用する酸無水物の疎水性を変化させることで、相分離挙動を制御することに成功しました ( Das E, Matsumura K., J. Poly,m. Sci. A., 2017 ) .
さらに、温度応答性やpH応答性などの、刺激応答性のポリマーとしてDDS用途への応用を目指した研究にも取り組んでいます ( Rajan, R, Matsumura K., Macromol. Rapid. Commun. 2017 ) 。

