常識にとらわれない新しい発想で医療に貢献する
私たち松村研究室では、「常識にとらわれない新しい発想で医療に貢献する」ことを目標に、材料科学と生命科学を融合した研究に取り組んでいます。
生体はとても複雑で繊細なシステムですが、その仕組みを理解し、材料の力でそっと支えることで、
これまで不可能と思われていた医療を実現できると私たちは信じています。
細胞を守る材料、薬を届ける材料、組織と一体化する材料を“ゼロからデザイン”し、
まったく新しい仕組みで治療を実現する――そのための挑戦を続けています。
細胞を壊さずに凍らせる高分子、タンパク質を変性から守る両性電解質ポリマー、体内でゆっくり溶けて組織になる足場、生体に優しいマイクロニードル…。
どれも「こんな材料があったらいいのに」という発想から生まれたものです。
研究室では合成化学、分析、細胞実験、材料設計、デバイス作製まで幅広く経験でき、学生が自ら発見し、自分のアイデアを形にできる環境を整えています。
挑戦を楽しめる人、新しい医療を一緒につくりたい人を歓迎します。
Research Themes
4つの研究テーマ
RESEARCH Theme 01
両性電解質高分子化合物を利用したバイオマテリアル
両性電解質高分子化合物を利用したバイオマテリアル
生体の大部分は水でできており、タンパク質や酵素は “水の中でどう振る舞うか” によってその働きが大きく変わります。
その複雑な世界を解き明かす手がかりとして、いま注目を集めているのが両性電解質高分子です。
プラスとマイナス、両方の電荷を持つという特殊な性質から、水と独特の関わり方をし、通常の高分子にはない現象を引き起こします。
松村研では、この “ちょっと変わった” 高分子のふるまいを徹底的に探り、
細胞を守る、薬を運ぶ、タンパク質を安定化する、生体と調和する―― そんな未来の医療材料へとつなげる研究を行っています。
1. 細胞凍結保護効果 (Cryoprotection)
松村研オリジナルの研究テーマで、細胞を “守りながら凍らせる” 革新的材料を開発しています。
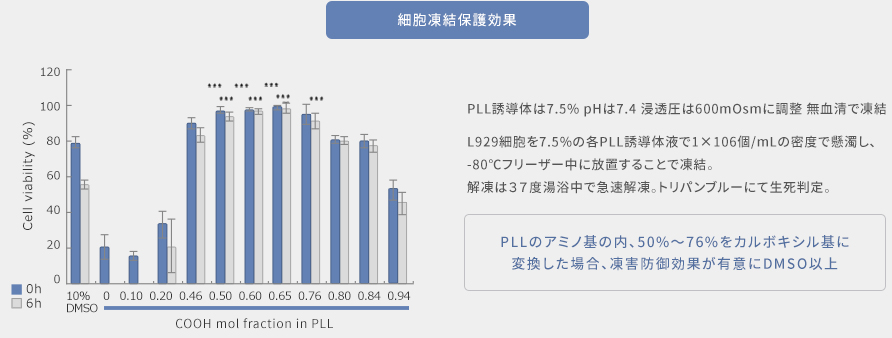
私たちが見出した両性電解質高分子は、従来のジメチルスルホキシド (DMSO) に代わる凍結保護剤となるポテンシャルを持っています。例えば、ポリリジンのアミノ基を一部カルボキシル基に変換したカルボキシル化ポリリジン (図1) (Matsumura K. et al., Biomaterials 2009) が高い細胞凍結保護作用を持つ事を最初に報告しました (図2)。
この高分子は種々の細胞の凍結保護に有効で、幹細胞やヒトiPS細胞の凍結保存にも有用であることを示しました。
(Matsumura K. et al., Cell Transplantation 2010, Matsumura K. et al., Cryobiology 2011)
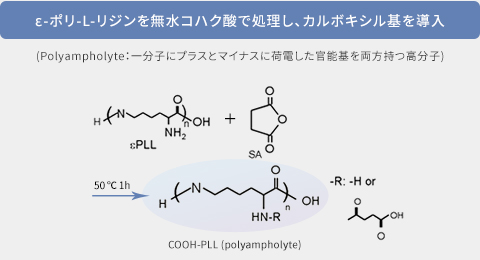
合成凍結保護高分子の設計
カルボキシル化ポリリジンだけでなく、プラスのモノマーとマイナスのモノマーを共重合させた、完全合成の両性電解質高分子にも凍結保護効果があることを報告しました (Rajan R., et al., J. Biomater. Sci. Polym. Ed., 2013) 。
たとえば、第3級アミノ基をもつモノマーとカルボキシル基を持つモノマーを共重合させた両性電解質高分子は、高い細胞凍結保護活性を持ちましたが、一方で、側鎖に両方の電荷を持つ双性イオン高分子(zwitterionic ppolymer) は高い活性を持ちませんでした。
その機序として、各ポリマーが持つ細胞膜親和性や、氷晶成長抑制効果の違いが関与していることがわかりました (Rajan R. et al., Biomacromolecules, 2016) 。また、ブチルメタクリレートなどの疎水性のモノマーを少量共重合することでさらに保護活性が向上することも報告しました (図3)。また近年では、細胞内に浸透するポリマーによる凍結保護効果も報告しています (Yamasaki R et al., Chem Commun., 2023) 。
このように、分子設計により、新しい凍結保護物質の最適化も可能となってきています。将来的には、細胞ごとに最適なテイラーメイドの凍結保護剤の開発も可能になるかもしれません。
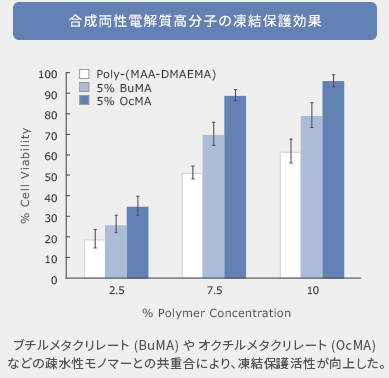
凍結保護の機序解明
それのみで細胞を高効率に凍結保存できるような高分子化合物はこれまでに報告されておらず、その機序の解明に興味が持たれます。
これは従来の概念とは異なる新しい凍結保護のアプローチであり、その仕組みを明らかにすることは学術的にも高い価値があります。
従来の凍結保護剤は細胞膜を通過し、細胞内の氷晶形成を抑える仕組みが主流です。一方、松村研が扱う両性電解質高分子は細胞内には入りません。
それでも細胞を守れる理由を科学的に解明するため、私たちは凍結状態そのものを観察できる固体NMR を導入しました。
固体NMRにより、0℃ 〜 -41℃ の範囲で、水分子の動き (運動性) 、Naイオンの拡散のしやすさ、凍結時の溶液粘性の変化などを観測出来ます。
解析の結果、両性電解質高分子 PLL-(0.65) 溶液では、低温になるほど水の動きが強く抑制され、溶液が粘性の高い状態になることが明らかになりました。これは、氷晶の成長を物理的に抑える働きと一致します。
さらに、PLL-(0.65) は高分子鎖に Na+ をトラップし、浸透圧を急激に上げないため、細胞の脱水が穏やかに進むという優れた特性も確認されました。
この効果は、ポリエチレングリコールやアルブミンなどの他の高分子化合物よりも遙かに高く、細胞凍結保護効果と一致することがわかりました。
固体NMRと細胞実験の結果から、松村研では “新しい凍結保護モデル” を提唱しています (図4)。
低温で高分子が水・塩を抱え込む「会合体」を形成する
その結果、水と塩の運動性が低下
→ 細胞外氷晶の成長が抑制され
→ 浸透圧変化が穏やかになり、細胞内の脱水が適切に進む
→ 最終的に細胞内への氷晶侵入が防がれ、細胞が守られる
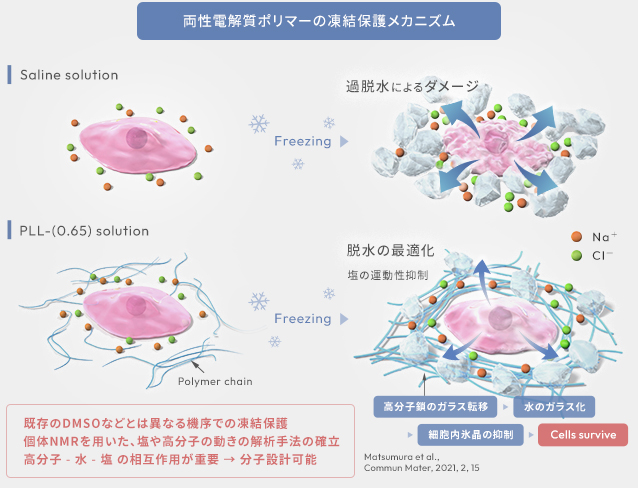
高分子が水や塩を分子間会合体中にトラップし、氷晶の伝播や急激な浸透圧上昇を防ぎ、
氷晶によるダメージや細胞内氷晶形成を抑制していると考えられる。
このメカニズムは、従来の「細胞内に浸透して守る凍結保護剤」とはまったく異なる全く新しい概念であり、
「高分子が細胞外環境を最適化することで細胞を保護する」という世界初の仕組みを明らかにした研究です (Matsumura K, et al., Commun Mater., 2021)。
再生医療への応用
再生医療の研究が広がるにつれ、細胞構造体の創出が容易になってきています。たとえば、細胞シートや再生皮膚、再生軟骨などの開発が盛んに行われ、
すでに臨床応用も行われています。iPS細胞などの幹細胞から組織を作成することが可能となりつつありますが、まだまだ時間がかかります。
そこで、できあがった組織をあらかじめ凍結してストックしておくという技術があると、必要な時に必要な組織をすぐに使用することができます。
そのような技術があれば、再生医療の産業化が見えてきます。
しかし、細胞懸濁液と異なり、細胞のシートや構造体は、細胞ー細胞間の相互作用があり、また大きな構造体であることから、一般的な -80℃に放置するという緩慢凍結法では生存率を維持できないという問題があります。そこで、受精卵などの凍結保存に用いられているガラス化法 (Vitrification) という手法に着目しました。
ガラス化法は、超急速凍結を行うことで、凍結時に水の結晶化を防ぎ、アモルファスのまま固化させるという手法です。この手法によると、細胞内外の水の体積膨張や、結晶による物理的ダメージなどを防ぐことができます。ただし、水は非常に結晶化しやすいので、結晶化を防ぐために高濃度の溶質、非常に速い凍結速度が要求されてきました。
両性電解質高分子化合物に、氷晶の成長を抑制するという研究成果が報告されました (Vorontsov D., et al., J. Phys. Chem. B., 2014) 。そこで、松村研では、カルボキシル化ポリリジンの氷晶成長抑制効果を調べ、より効果的なガラス化保存液の開発を行っています。具体的には、低濃度の溶質でより簡便に誰でもできる手法を開発し、それを再生医療用の細胞構造体の凍結へ応用したいと考えています。
応用例としては、
軟骨シートのガラス化 Maehara M., et al., BMC Biotechnol., 2013
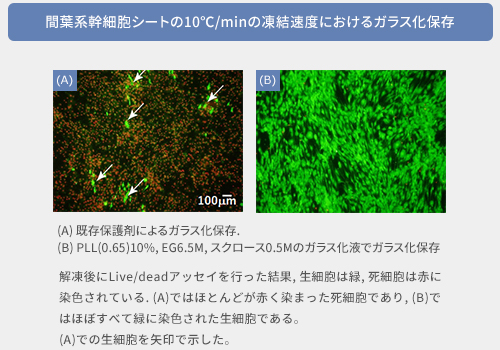
間葉系幹細胞シートのガラス化 Matsumura K., et al., ACS Biomater. Sci. Eng., 2016 (図5) 等があります。
さらに、3Dスフェロイドの「凍結ではなくガラス化保存」も独自に成功し、液体窒素を使わずに -150℃ で保存できる技術も確立しました (Matsumura K, et al., Biomacromolecules, 2020) 。
再生医療や細胞輸送の常識を塗り替える、新しい細胞保存プラットフォームの実現を目指しています。
2. タンパク質保護高分子 (Protein protection)
タンパク質は生命活動の中心となる分子であり、酵素反応、ホルモン伝達、免疫応答など、あらゆる生体機能を担っています。
しかし、タンパク質は非常に繊細で、熱・乾燥・pH変化・凍結融解・力学的刺激といったわずかな環境変化によって容易に変性し、本来の機能を失ってしまいます。
医薬品や診断試薬としてタンパク質を扱う際、この「不安定さ」は最大の課題の一つです。
松村研究室では、この問題を根本から解決するために、タンパク質を“守る”高分子の設計に取り組んできました。特に注目しているのが、強い水和構造と優れた生体適合性を示す 両性電解質高分子やスルホベタイン系双性イオン高分子です。これらの高分子は分子全体で厚い水の層を保持し、「水のバリア」をまとっているような状態になります。この水和層がタンパク質の周囲に穏やかな環境を提供し、外部ストレスからタンパク質を守る“天然の保護膜”のように働きます。
実際、両性電解質高分子はタンパク質表面に非特異的に吸着することなく、その近傍の水の動きを整えることで 凝集の抑制 や 熱安定性の向上 をもたらすことが明らかになりました (Rajan R., et al., J. Mater. Chem. B, 2015)。
図6にあるように、ポリスルホベタインを添加した場合、リゾチームを90℃で30分熱しても凝集塊ができずに、酵素活性を維持していることがわかりました。この作用は、ポリスルホベタインをナノゲルにしたり、疎水性基を導入することでさらに増強することもわかり (Rajan R, Matsumura K., Sci. Rep., 2017) 、様々なタンパク質・酵素の凝集抑制作用について応用展開が考えられます。
これは、従来の添加剤が「タンパク質と直接結合して安定化する」のとは異なる、“水分子を介した間接的な保護”という革新的なメカニズムです (図7) (Rajan R., et al., Cell Rep. Phys. Sci., 2024)。

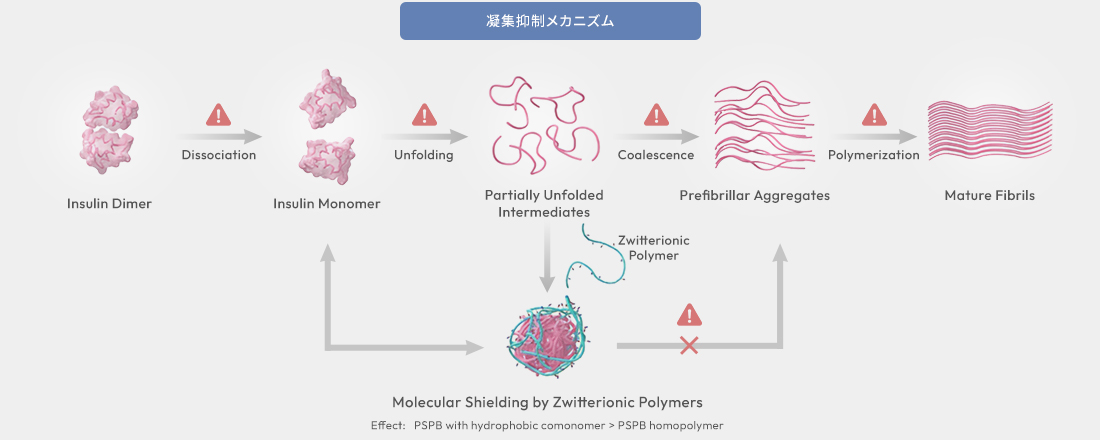
インスリン二量体(天然構造)が加熱により単量体に変性し、さらにアンフォールディングして立体構造が解消される。その際にポリマーがあると、分子シールディング効果 により、凝集前駆体の形成を抑制し、繊維状凝集前駆体(prefibrillar aggregation)から繊維凝集体 (Mature fibrils)の形成を阻害する。
さらに、タンパク質保護高分子の大きな応用先として、バイオ医薬品の安定化があります (Rajan R. et al., Macromol. Biosci., 2018, Sharma N. et al., ACS Omega 2019)。酵素製剤、抗体医薬、ワクチンなどは非常に高価で、保存や輸送には厳密な温度管理が必要です。もし室温で安定に保存できるようになれば、医薬品の物流・供給体制に大きなイノベーションをもたらすことができます。また、診断用酵素や抗体の安定化にも応用でき、医療・検査の現場での取り扱いが格段に容易になります。
松村研では、ポリマーの電荷構造・水和力・疎水性のバランスを分子レベルで調整し、タンパク質の種類や目的に応じた最適な保護材料を設計しています。
中には、乾燥状態でもタンパク質の構造を維持できる材料や、凍結融解を繰り返しても活性を失わない材料も報告されています。
また、ポリマーをナノ粒子化したり、ゲルマトリックスに組み込むことで、酵素カプセル化やDDS(ドラッグデリバリーシステム)との統合も可能になります。
これら研究テーマの魅力は、化学と生命科学の密接なつながりを実感できる点です。
分子の水和構造というミクロな現象が、タンパク質の安定化というマクロな機能につながり、その成果が医薬品や診断試薬といった社会的インパクトのある応用へ直結します。高分子合成、NMR・DSCなどの物性解析、タンパク質評価、機能測定まで幅広い技術を横断的に学ぶことができます。