生体組織と調和する生体材料の開発
― 分子構造から“使える医療材料”を設計する
生体材料に求められる最も重要な条件は、「生体と調和すること」です。体内で異物として拒絶されず、長期間にわたって安定に機能し、必要に応じて力を支え、細胞や組織と共存できることが不可欠です。松村研究室では、高分子の分子構造・水和状態・力学特性を精密に制御することで、生体と本質的に相性のよい材料を設計することを目指しています。
その代表的な研究テーマの一つが、ポリビニルアルコール(PVA)ハイドロゲルです。PVAは高い生体適合性、低毒性、化学的安定性を持つことから、 コンタクトレンズや人工軟骨、組織工学用足場材料として古くから研究されてきました。特に、化学架橋剤を使わず、水素結合による「物理架橋」で形成されるPVAハイドロゲルは、生体材料として理想的な特徴を備えています。
しかし、従来よく用いられてきた 凍結融解(Freeze-Thaw)法 には課題がありました。凍結時の氷晶形成によって相分離が起こり、ハイドロゲルが白濁し、力学強度も十分ではありません。さらに、長期使用時には結晶構造の変化や劣化が懸念されてきました。
有機溶媒を使わない「ホットプレス法」によるPVAハイドロゲル
松村研究室では、これらの課題を克服するため、有機溶媒を一切使用しないホットプレス法によるPVAハイドロゲルの作製に取り組んできました (Sagkaguchi T. et al., Polymer J. 2017)。また、リチウム塩添加による熱可塑性付与、マイクロ結晶制御など、材料工学の深い知見と医療ニーズを統合する研究が進んでいます (Taoka Y., et al., ACS Omega, 2023, Taoka Y., Macromol Chem. Phys., 2025)。
さらに近年の研究では、通常用いられるアタクチックPVA(aPVA)ではなく、シンジオタクチック性の高いPVA(sPVA)に着目しました(Taoka Y., RSC Appl. Polym., 2025)。
sPVAは側鎖の配置が規則的で結晶化しやすく、本来は非常に優れた力学特性を持つ材料です。しかし、その高い結晶性ゆえに水やDMSOにも溶けにくく、従来法ではゲル化が困難でした。そこで本研究では、PVAを溶かさず、水で膨潤させた状態のまま高温・高圧で成形するホットプレス法を適用することで、sPVAハイドロゲルの作製に成功しました。
この方法により得られた sPVA ハイドロゲルは、高い結晶性から、安定なゲル構造を示し、高い力学的強度を持ちます。以下のような特長を示します。
特に注目すべき点は、sPVAハイドロゲルが aPVAでは180℃の熱処理が必要な力学特性を、100℃程度の低温処理で達成できる ことです。これは、分子レベルでの規則正しい構造(高いタクティシティ)が、効率的な結晶化と強固な物理架橋を可能にしているためです。
人工軟骨材料には、「生体軟骨に近い摩擦特性」「高い耐久性」「長期安定性」が同時に求められます。sPVAハイドロゲルは、生体親和性の高さに加え、微結晶構造による強固なネットワークを持つため、生体組織と機械的にも調和する材料として大きな可能性を秘めています (図16)。

生体と“対立しない”材料設計へ
松村研究室の生体材料研究の根底にあるのは、「生体を無理に制御するのではなく、生体の環境や性質に寄り添う材料設計」です。
PVAハイドロゲル研究では、分子の立体規則性(タクティシティ)水との相互作用結晶と非晶のバランス力学特性と生体適合性の両立といった要素を分子レベルで理解し、“なぜこの材料は生体と調和するのか” を科学的に説明できる材料設計を行っています。
この研究テーマでは、高分子合成、構造解析(NMR・FT-IR・XRD)、熱分析、力学試験といった幅広い実験手法を学ぶことができ、基礎から応用まで一貫して取り組むことができます。
抗がん高分子(Polymeric Anticancer Agents)
がん治療は長年にわたり「抗がん剤(低分子薬)」が中心でした。しかし、従来の抗がん剤は正常細胞も攻撃してしまうため、副作用が大きく、薬剤耐性の問題も避けられません。その一方で、がん細胞が本質的に持つ性質──たとえば表面電荷、膜構造、代謝特性──を利用すれば、まったく新しい治療アプローチを生み出すことができます。
松村研究室が取り組んでいるのは、「薬物そのものではなく、高分子が直接がん細胞を攻撃する」という新しい抗がんコンセプト です。つまり、化学的に設計したポリマーが、薬剤なしでがん細胞を殺傷する「高分子自体が薬になる」という発想です。
その鍵となるのが、疎水基を導入したポリカチオンです。がん細胞の膜は、正常細胞に比べて負電荷を多く帯びており、さらに膜流動性が高く、外部物質に対して脆弱な面があります。松村研では、このがん細胞膜の特徴に着目し、正電荷(カチオン)による静電吸着 × 疎水基による膜挿入 を組み合わせた高分子を設計しました。
このポリカチオンは、まず正電荷ががん細胞の負電荷部位に強く引き寄せられ、次に疎水基が細胞膜の内側に突き刺さるようにして挿入されます。結果として、膜の秩序構造が乱れ、膜透過性が急激に上昇します。論文では、この高分子が がん細胞膜を崩壊させる ことが示されています。これは抗がん剤のように細胞の内部の代謝を阻害するのではなく、外側の膜を直接破壊するため、薬剤耐性が生じにくい点が大きな利点です (図17, Kumar N., et al., J. Mater. Chem. B, 2023)。
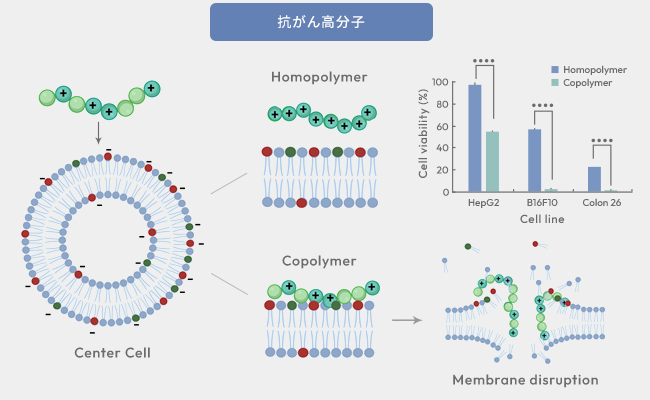
高分子のカチオン性部位と疎水性部位ががん細胞の細胞膜をアタックし、膜障害により抗がん効果を示す。
さらに興味深いのは、この膜破壊作用が正常細胞よりがん細胞に強く現れる点です。がん細胞は膜の負電荷が高く、また構造的に弱くなっているため、ポリカチオンがより選択的に作用するというメカニズムが確認されています。この選択性は、従来の化学療法では得にくい“安全性の高さ”につながる可能性があります。
また、松村研ではポリマーの電荷密度・疎水基の長さ・分岐構造・主鎖柔軟性を精密に変化させ、最も効果的に膜破壊を誘導できる分子設計を探索しています。たとえば、疎水基が強すぎると正常細胞にも影響を与えてしまい、弱すぎるとがん細胞膜に挿入できない──そのバランスを取るための分子設計が重要です。また、高分子の長さや結合様式によって細胞膜との相互作用が劇的に変化することも実験で示されています (図18, Kumar N, et al., Biomacromolecules, 2024, Kumar N., et al., Mater. Adv., 2024, Shahid, MH., et al., Royal Soc. Open Sci., 2025)。
この研究分野は、化学・材料科学・細胞生物学が密接に組み合わさった高度な領域であり、学生は 高分子合成、界面科学、膜物性解析、細胞毒性試験、ライブセル観察、顕微鏡解析 など多彩なスキルを身につけることができます。とくに、膜破壊メカニズムを蛍光顕微鏡で追跡する実験は視覚的にも興味深く、研究の面白さを強く実感できるでしょう。