ドラッグデリバリーシステム(DDS)に関する研究
物質を適切な場所に送り届ける薬物送達技術や、生体内で必要な分量の放出を制御する薬物徐放技術など、ドラッグデリバリーシステムの研究は幅広く行われて います。当研究室では、薬物の徐放技術や細胞内への送達技術について独自の観点から研究を行っています。
凍結濃縮を利用した細胞内物質導入(Intracellular Delivery)
細胞の膜を壊さずに内部へ薬物・タンパク質・核酸などを届ける技術を研究しています。
特にユニークなのが「凍結濃縮(Freeze Concentration)」を利用した導入法です。 細胞と薬物を一緒に軽く凍らせることで、溶質濃度が細胞表面に一気に高まり、効率的に取り込まれます。
細胞内にタンパク質や遺伝子を入れることは、細胞治療のためのドラッグデリバリーシステムの重要な課題です。細胞膜は疎水性の脂質二重膜から出来ており、容易に親水性の物質を透過させません。しかし、細胞はレセプターなどを利用してエンドサイトーシスという作用で細胞外から物質を取り込むことを行っています。
松村研究室では、全く独自の観点からこの物質の細胞内への取り込み向上に成功しています。一般に、水溶液を凍結すると、氷結晶は純粋な水の結晶であるため、溶質成分を残存溶液部位の押し出すことで、残存水が濃縮されることが起こります。
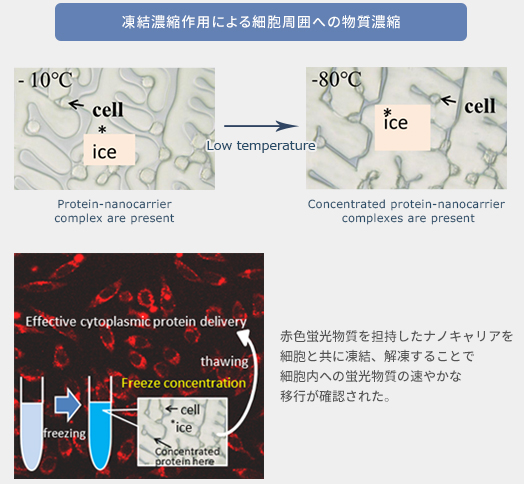
これを凍結濃縮と呼び、ジュースの凍結時に、濃い部分と薄い部分に分かれる現象などで知られています。この現象を細胞懸濁液でも引き起こすことで、細胞周囲に物質を濃縮することが可能です。すなわち、細胞凍結保護物質の存在下で、細胞膜と親和性の高いナノキャリアに目的の物質を封入し、添加しておきます。その懸濁液を凍結すると、細胞が存在する残存水の濃度が急激に上昇します。
その時に細胞周囲にナノキャリア複合体も濃縮され、細胞膜に吸着します。その後、解凍すると、細胞膜親和性のナノキャリアは細胞膜に吸着したままとなり、細胞はエンドサイトーシス作用により取り込みます。このように、一旦凍結するだけで細胞内に物質を効率よく取り込むことが出来るのです (図11, Ahmed S et al., Biomaterials 2014) 。
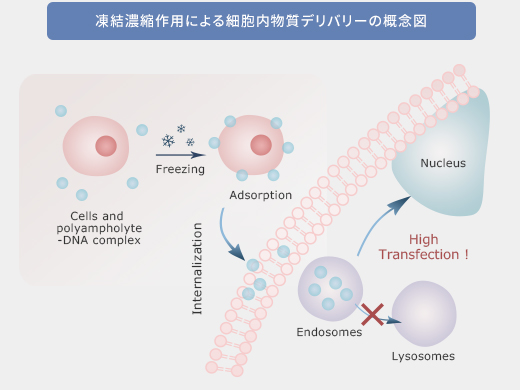
ナノキャリアに両性電解質高分子を組み込むことで、細胞が取り込んだ後、物質を消化するエンドソームから脱出する作用を付与する事が可能となり、目的部位への到達度の向上にも成功しました (Ahmed S et al., Nanoscale 2016) 。
この手法は、抗原導入 (Adv. Healthc Mater 2017) 遺伝子導入 (ACS Biomater Sci Eng 2017) 、金ナノ粒子 (Biomat Sci 2018) などの導入にも成功しています (図12) 。
基礎的な検討として、凍結保護物質に我々のポリマーを用いることでさらに高い凍結濃縮度が得られること (Langmuir 2018) 、未凍結の低温においてリポソームへの金ナノ粒子の取り込みが向上する (Langmuir 2019) など、興味深い知見が多く見つかっております。
遺伝子治療・免疫治療など幅広い応用が期待されます。このような凍結技術のバイオマテリアルへの応用に関しての研究は総説としてまとめています (Matsumura K, et al., Polymer J, 2023)。
温度応答性DDS(Thermoresponsive DDS)
細胞の中では、タンパク質や核酸が液滴のように集まり、膜のない小器官(液–液相分離構造、LLPS)を形成することが知られています。 この 「相分離(Phase Separation)」 は、生命現象を支える重要な仕組みであり、分子が環境変化に応じて“自発的に集まり・離れる”という高度な自己組織化の表れです。
松村研究室では、この相分離現象を高分子材料に応用し、薬を必要なときにだけ放出する新しいDDS(ドラッグデリバリーシステム) の開発に取り組んでいます。
特に、正負の電荷を併せ持ち、水との強い相互作用を示す 両性電解質高分子 は、温度・塩濃度・電荷バランスに敏感で、環境変化に応じて相分離を起こしやすいという特徴を持ちます。これに分子設計を加えることで、温度応答性を自在に調整できるようになります。
この温度応答性高分子の代表例は、温めると水に溶けにくくなり、急激に相分離して“濃縮相(薬を閉じ込める部分)”と“希薄相(周りの水)”に分かれる材料です。相分離した瞬間、薬物は濃縮相に取り込まれ、その後の環境変化(温度・光刺激)によって制御されたタイミングで放出されるため、“オンデマンド薬物放出” が可能になります(図13, Das E., et al., J. Polym. Sci A, 2017, Hirose T., et al., MSDE, 2024)。
松村研ではさらに、共役系高分子、液体金属ナノ粒子などの光加熱材料を組み合わせ、「光 → 局所加熱 → 相分離 → 薬物放出」 という高度な制御システムを構築しています(温度応答性DDS)。 近赤外レーザー光を当てた部分だけがわずかに温度上昇し、その局所的な温度変化が高分子の相分離トリガーとなるしくみです。これにより、副作用を減らしながら“必要な場所に必要な量だけ薬物を届けられる”極めて高精度なDDSが実現します(図14)。
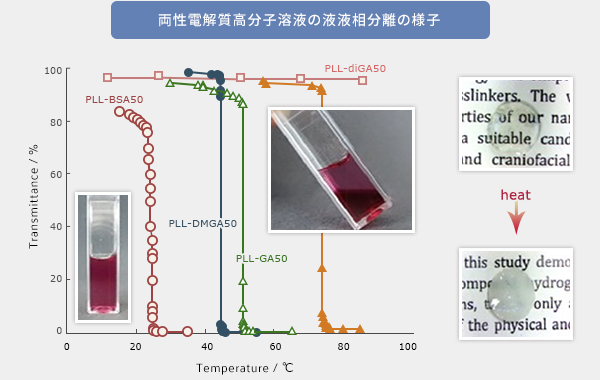
熱をかけると上部に希薄溶液、下部に濃縮溶液の二層に分離する。
ゲル化させると加熱により収縮、白濁する。

特殊な共役系高分子(ドナーアクセプター高分子のナノ粒子(TEM画像)の水分散液に波長808nmの近赤外光を照射することで発熱することを確認。
温度応答性高分子と組み合わせることで、熱による薬物の徐放を期待。
このアプローチには、次のような大きな利点があります。
① 空間的に狙った位置だけで薬物を放出できる
光刺激は局所性が高いため、周囲の正常細胞を傷つけず、がん細胞や患部など特定場所だけを標的化できます。
② 放出タイミングを何度でも制御できる
温度応答性高分子の相分離は可逆的なため、刺激→相分離→放出→再溶解を繰り返すことができ、持続的な治療に向いています。
③ 生体環境の影響を受けにくい
pH やイオン濃度の影響を受けにくい“温度”をスイッチとして利用するため、体内環境の個体差に左右されにくい高い安定性を持ちます。
さらに、両性電解質高分子はもともと高い親水性・生体適合性を持つため、薬物の安定化や副作用低減にも寄与します。松村研では、分子設計(疎水基導入、芳香環導入、電荷比の調整)によって相分離温度の微調整にも成功しており、室温〜生理温度〜レーザー加熱など、多様な治療環境に合わせた材料設計が可能です (Zhao D., et al., ACS Appl. Mater. Interfaces, 2019)。
この研究は、高分子化学・ソフトマター物理・ナノ材料・医用工学 が融合する最先端領域であり、学生は分子設計から物性解析、細胞実験、薬物放出評価まで幅広い技術を学ぶことができます。
経皮ドラッグデリバリーシステム − マイクロニードル
「貼るだけで薬が入る」――そんな夢のような治療技術として注目されているのが マイクロニードル(Microneedle) です。
マイクロニードルは、皮膚表面にある“痛覚を持たない浅い層”だけをわずかに貫通する、非常に細く短い針状のデバイスです。注射のような痛みや不快感がなく、かつ皮膚バリアを越えて薬物を効率よく届けることができるため、ワクチン、インスリン、抗体医薬、タンパク質製剤、ペプチド薬など、多様な分野で開発が進んでいます。
しかし、マイクロニードル技術にはいくつかの課題があります。たとえば、高分子タンパク質や酵素のようなデリケートな薬物は製剤化の過程で変性しやすく、熱・乾燥・界面などのストレスに弱いため「マイクロニードルに薬を入れた時点で活性が失われてしまう」ことがあります。また、皮膚中で針が確実に溶け、薬物を適切な速度で放出させるためには、材料の構造・水和性・溶解性などの緻密な設計が必要です。
松村研究室では、これらの課題を解決するために、高親水性でタンパク質保護能力の高い両性電解質高分子を基盤とした 高分子マイクロニードル を開発しています。とくに、スルホベタイン系ポリマー(poly-SPB)は、強い水和構造を持つためにタンパク質の凝集を抑え、乾燥工程でも活性を高く保てることがわかっています。この性質を活かして、タンパク質・酵素・ペプチドなど、敏感な医薬成分の活性を保ったまま皮膚に送達できるマイクロニードル を実現しました(図15, Pitakjakpipop H., et al., Biomacromolecules, 2021)。
加えて、松村研では光リソグラフィー技術や刺激応答性高分子などを応用し、数十マイクロメートル単位で形状を制御したマイクロニードルを作製しています( Supachettapun C., et al., J. Mater. Chem. B, 2025)。微細な形状制御により、皮膚への挿入効率を高め、患者間の個体差や部位差に左右されにくい安定した送達性能を実現しています。
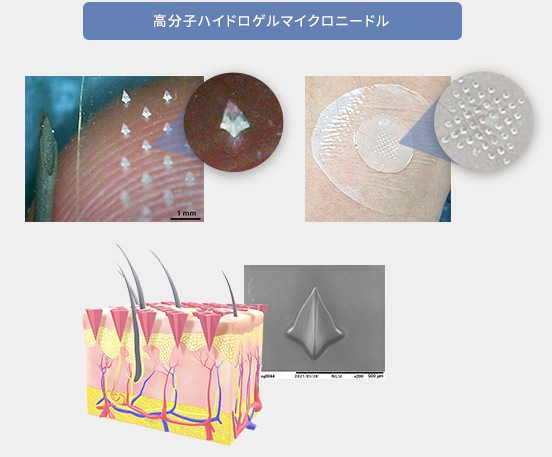
フォトリソグラフィーの手法で作成した高分子ハイドロゲルマイクロニードル。 そのSEM画像により1mm以下の短い針が確認された。 これは皮膚の痛点に届かないため、痛みを感じない針であり、経皮DDSが期待出来る。
この研究テーマでは、材料合成、フォトリソグラフィーによる微細加工、タンパク質安定化評価など、幅広いスキルを習得できます。
マイクロニードルは世界中で研究・製品化が進む最先端分野であり、「貼るワクチン」「貼るインスリン」「貼る酵素治療」 といった新しい治療概念を生み出せる、大きな可能性をもった技術です。